
تولید دارو به فرآیند صنعتی در مقیاس صنعتی برای تبدیل مواد خام به داروهای نهایی اشاره دارد.. به عبارت دیگر, این نحوه تولید قرص توسط شرکت های دارویی است, کپسول ها, تزریقی و سایر اشکال دارویی تحت شرایط کاملاً کنترل شده. این فرآیند شامل یک سری مراحل دقیق است - از مخلوط کردن و مخلوط کردن مواد شیمیایی تا تشکیل قرص ها و بسته بندی آنها - همه برای اطمینان از ایمن بودن داروهای نهایی طراحی شده اند., موثر, و با کیفیت بالا. همانطور که پتی فو اشاره می کند, تولید دارو «فرایند سنتز در مقیاس صنعتی است, آماده سازی, و بسته بندی داروها و فرآورده های دارویی. در عمل, این به معنای تبدیل مواد فعال دارویی است (API ها) و مواد کمکی به اشکال دوز (مثل تبلت ها, کپسول ها, مایع, یا تزریقی) از طریق انواع عملیات واحد (آسیاب, دانه, تراکم, پوشش, پر کردن آسپتیک, و غیره) تحت مقررات سختگیرانه. هدف نهایی تولید داروهای قابل اعتماد در مقیاس بزرگ در عین رعایت تمام استانداردهای بهداشتی و ایمنی است.
تولید دارو فقط اختلاط تصادفی مواد شیمیایی نیست - این یک فرآیند بسیار مهندسی شده است.. در هسته آن, شامل می شود: شناسایی یا سنتز یک ماده دارویی فعال (API), ایجاد یک فرمول پایدار با مخلوط کردن API با مواد دیگر (بنده, پرکننده, حلال ها, و غیره), و سپس این ترکیب را به شکل دوز نهایی پردازش کنید. هر عملیات (مخلوط کردن, دانه, خشک شدن, فشرده سازی, پوشش, پر کردن, و غیره) باید با دقت انجام شود. FDA و سایر آژانسها با تمام این فرآیند بسیار جدی برخورد میکنند - هر دسته باید معیارهای دقیق هویت را داشته باشد, قدرت, خلوص, و کیفیت. به طور خلاصه, تولید دارو ستون فقرات صنعت دارو است, استفاده از ماشین آلات تخصصی و محیط های کنترل شده برای تبدیل ایمن و کارآمد مواد شیمیایی به دارو.

تولید دارو یکی از مقرراتی ترین صنایع در جهان است. چرا? زیرا ما در حال تولید محصولاتی هستیم که مردم تزریق میکنند یا میبلعند, بسیار مهم است که هر دوز دقیقاً درست و عاری از آلودگی باشد. مقررات (به ویژه GMP - شیوه های تولید خوب) برای اطمینان از ایمنی بیمار و کیفیت ثابت محصول وجود دارد. به عنوان مثال, مقررات FDA ایجاب می کند که سازندگان دارو از شیوه های فعلی تولید خوب پیروی کنند (CGMP), که دستورالعمل هایی برای اطمینان از اینکه محصولات "به طور مداوم مطابق با استانداردهای کیفیت تولید و کنترل می شوند" هستند.. هدف این است که هر دارویی را تضمین کند:

به طور خلاصه, چون زندگی مردم در خط است, تولید دارو توسط قوانین سختگیرانه آژانس هایی مانند FDA اداره می شود, EMA, و WHO. این قوانین همه جنبه ها را پوشش می دهد - طراحی تاسیسات, تجهیزات, آموزش پرسنلی, تست مواد خام, ثبت سوابق, تمیز کردن, اعتبار سنجی, و بیشتر. از این طریق, تنظیم کننده ها کمک می کنند تا اطمینان حاصل شود که هر قرص یا ویال که به دست بیماران می رسد به گونه ای ساخته شده است که "اطمینان حاصل شود که یک محصول برای استفاده ایمن است".
مسیر از شیمی خام تا پزشکی نهایی شامل چندین مرحله کلیدی است. در حالی که فرآیندهای خاص بسته به محصول متفاوت است, یک گردش کار معمولی تولید دارو شامل این مراحل اصلی است:
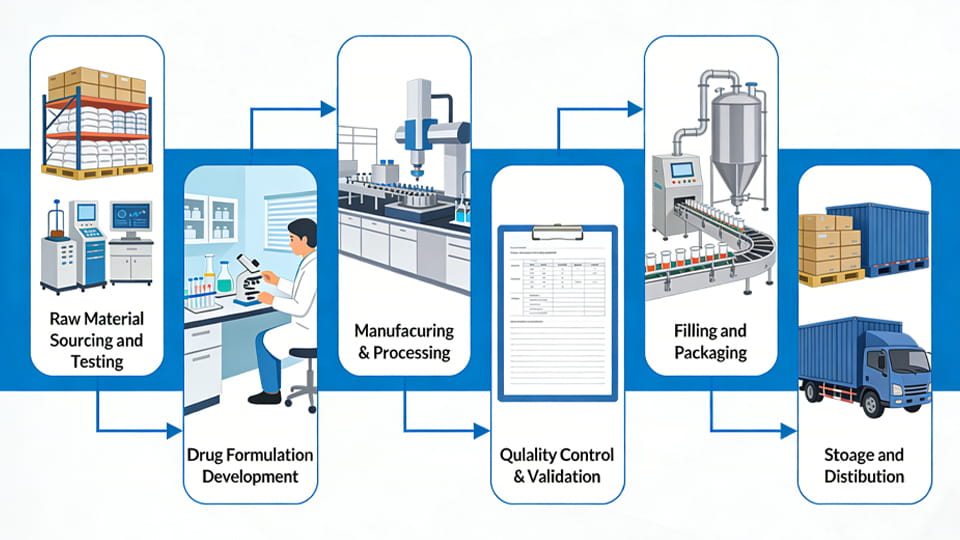
در تمام این مراحل, پایبندی دقیق به GMP اعمال می شود. از ممیزی تامین کنندگان در مرحله 1 به بررسی های عقیمی در مرحله 6, کیفیت در هر مرحله ساخته شده است. این فرآیند چند مرحله ای - از مواد اولیه تا تحویل نهایی - تولید داروسازی مدرن را تعریف می کند..
گیاهان دارویی را می توان به روش های مختلف بسته به محصول و مقیاس سازماندهی کرد. انواع اصلی رویکردهای تولید عبارتند از:
به طور سنتی, اکثر محصولات دارویی به صورت دسته ای ساخته شده اند. در یک فرآیند دسته ای, یک مقدار ثابت (دسته ای) محصول از ابتدا تا انتها تولید می شود. هر مرحله قبل از حرکت به طور جداگانه در یک دسته اجرا می شود. به عنوان مثال, یک فرمول در یک مخزن بزرگ مخلوط می شود, دانه بندی شده, خشک شده, به صورت قرص فشرده شده است, و سپس آن دسته از قرص ها بسته بندی و آزمایش می شود. مزیت تولید دسته ای انعطاف پذیری است: تغییر فرمولاسیون یا تغییر مرحله برای محصول جدید نسبتاً آسان است. کارخانههای داروسازی اولیه از این امر استقبال میکردند، زیرا تغییرات فرآیند ساده و مستندات ساده را امکانپذیر میکرد. تولید دسته ای شامل هر عملیاتی است که به طور جداگانه با استفاده از مقدار مشخصی از مواد اجرا می شود, با بررسی های میانی بین فازها. در عمل, این بدان معنی است که پس از یک مرحله انجام می شود, مواد قبل از ادامه نمونه برداری و آزمایش می شود.
جوانب مثبت تولید دسته ای: آسان برای تغییر محصولات یا اندازه دسته, کنترل فرآیند ساده و قابلیت ردیابی, ایده آل برای اجراهای کوچکتر یا زمانی که تعویض های مکرر مورد نیاز است.
معایب تولید دسته ای: معمولاً برای حجم زیاد - بعد از هر دسته - کندتر و کارآمدتر است, تجهیزات باید تمیز شوند و برای دستگاه بعدی تنظیم شوند. دست زدن بیشتر به صورت دستی احتمال خطای انسانی را افزایش می دهد. «عملیات متعددی برای رسیدگی لازم است, ذخیره, و نظارت بر محصولات میانی» در حالت دسته ای. همچنین, اگر اشتباهی در پایان یافت شود, کل دسته ممکن است از بین برود (برای مثال, یک خطای برچسب یا یک QC ناموفق در تبلتها میتواند باعث شود همه تبلتهای آن دسته حذف شوند).
یک رویکرد نوظهور است ساخت مداوم. به جای دسته های مجزا, ساخت مداوم باعث می شود مواد در هر مرحله بدون وقفه در جریان باشند. مواد اولیه در یک انتهای خط تولید وارد می شود و محصول نهایی دائماً از سر دیگر خارج می شود. کلیه عملیات واحد (مخلوط کردن, دانه, تراکم, و غیره) در یک خط تحت کنترل زمان واقعی یکپارچه شده اند. فرآیندهای پیوسته بسیار خودکار هستند, با سنسورهای درون خطی برای اندازه گیری پارامترها (مانند یکنواختی مخلوط یا سختی قرص) در پرواز. مزایا شامل توان عملیاتی بسیار بالاتر است, زمان تولید کوتاه تر, و کیفیت ثابت تر. تولید مستمر زنجیره تامین را بهینه می کند, استحکام فرآیند تولید را افزایش می دهد و در نتیجه خرابی محصول را کاهش می دهد. در واقع, تحقیقات نشان می دهد که پردازش مستمر می تواند بسیاری از هزینه ها را به نصف کاهش دهد - کاهش تنوع محصول, زمان کنترل کیفیت, و مصرف انرژی با حاشیه های زیاد (برآوردها از 40% به 70% کاهش می دهد). به عنوان مثال, زیرا مواد به حرکت خود ادامه می دهند, مشکلات فقط بر بخش کوچکی از محصول تأثیر می گذارد: هر بخش خارج از مشخصات را می توان منحرف کرد در حالی که بقیه ادامه دارد. سازمان های نظارتی (FDA, EMA, و غیره) به طور فزاینده ای از تولید مداوم حمایت می کنند - در 2022 ICH حتی دستورالعمل هایی را منتشر کرد (Q13) برای تشویق پذیرش آن.
مزیت های تولید مستمر: راندمان و توان عملیاتی بیشتر, مداخلات دستی کمتر, محصول نهایی یکنواخت تر, و اغلب ردپای تولید کوچکتر. نظارت بر کیفیت در زمان واقعی به این معنی است که مشکلات بلافاصله شناسایی می شوند. همچنین به سادگی با اجرای خط طولانی تر یا افزودن خطوط موازی، امکان افزایش سریع مقیاس را فراهم می کند.
معایب تولید مستمر: نیاز به سرمایه گذاری سنگین در جدید, تجهیزات یکپارچه و سیستم های کنترل. تغییر محصولات یا دستور العمل ها سخت تر است زیرا خط برای یک فرآیند خاص بهینه شده است. برای تغییر از یک دسته اثبات شده به یک راه اندازی پیوسته، اعتبار فرآیند و تأیید نظارتی گسترده مورد نیاز است (شرکت ها باید ثابت کنند که فرآیند جدید همان نتیجه را به همراه دارد). همانطور که اشاره شد, پذیرش تا حدی به دلیل این چالش ها کند بوده است.
| جنبه | تولید دسته ای | تولید مستمر |
|---|---|---|
| سبک تولید | اجراهای گسسته لات به لات | در حال انجام است, جریان بی وقفه |
| انعطاف پذیری | بالا - به راحتی محصولات یا اندازه دسته را تغییر می دهند | پایین - بهینه شده برای یک محصول, تغییرات کمتر |
| توان عملیاتی | کمتر - زمان خرابی بین دسته ها مورد نیاز است | بالاتر - خروجی ثابت, زمان تحویل کوتاه تر |
| کنترل کیفیت | نمونه برداری و آزمایش مرحله به مرحله | نظارت درون خطی و کنترل بازخورد |
| ریسک تغییرپذیری | بالاتر - هر دسته می تواند با آخرین بسته متفاوت باشد | سازگاری داخلی پایین تر (در صورت مشکل فقط بخش کوچکی از بین می رود) |
| محصولات نمونه | بسیاری از داروهای قدیمی, دسته های با حجم کم, لوازم بالینی | اشکال دوز جامد با حجم بالا (قرص ها, کپسول ها), API ها بر اساس شیمی جریان |
تمایز کلیدی دیگر این است که آیا محصول باید استریل باشد یا خیر. تولید استریل در مورد تزریقی اعمال می شود (واکسن ها, داروهای IV, قطره چشم) و قابل کاشت. این محصولات هیچ گونه آلودگی میکروبی را تحمل نمی کنند. در نتیجه, خطوط دارویی استریل تحت شرایط بسیار سخت اجرا می شود (اتاق های تمیز درجه بالا, فیلتراسیون هوا, تجهیزات استریل شده). به عنوان مثال, مواد تزریقی اغلب به محیط تمیز ISO-5 نیاز دارند (کلاس A/B در شرایط GMP اتحادیه اروپا) و فرآیندهای پر کردن آسپتیک. هر ویال یا سرنگ در زیر هودهای جریان آرام استریل یا در ظروف از پیش استریل شده پر می شود., و اجزاء (سوزن ها, فیلترها) ضدعفونی می شوند. در مقابل, تولید غیر استریل شامل محصولاتی مانند قرص است, کپسول ها, پماد, و مایعات خوراکی که محدودیت های قابل قبولی برای محتوای میکروبی دارند (توسط استانداردهای دارویی اداره می شود). خطوط غیر استریل هنوز بسیار تمیز هستند, اما آنها به شرایط کامل آسپتیک نیاز ندارند. کنترلهای کیفیت بیشتر بر یکنواختی و ثبات تمرکز دارند تا عقیمی مطلق. خلاصه, فرآیندهای استریل پیچیده تر و پرهزینه تر هستند (به دلیل استریلیزاسیون اضافی و نیازهای اتاق تمیز), در حالی که فرآیندهای غیر استریل, در حالی که هنوز تنظیم شده است, تا حدودی ساده تر هستند.
تولید دارو را نیز می توان بر اساس شکل دوز طبقه بندی کرد:
هر نوع (جامد, مایع, قابل تزریق) تفاوت های ظریف فرآیندی خود را دارد, اما همه باید با GMP مطابقت داشته باشند. انتخاب نوع تولید بستگی به شکل و کاربرد دارو دارد. به عنوان مثال, واکسن ها (قابل تزریق) فرآیندهای استریل پیچیده تری نسبت به قرص برای استفاده خوراکی انجام دهید.
تولید داروسازی مدرن بر مجموعه وسیعی از ماشین آلات تخصصی متکی است. تجهیزات به طور کلی در این دسته بندی ها قرار می گیرند:
هر قطعه از تجهیزات برای مطابقت با استانداردهای دارویی طراحی شده است (قطعات تماس فولاد ضد زنگ, توانایی تمیز کردن آسان, و غیره). تولید کنندگان پیشرو تجهیزات دارویی (مانند Jinlupacking) تولید ماشین آلات مانند پرس تبلت, پرکننده های کپسول, تاول بسته کننده ها, ماشین های شمارش, کارتن سازها, و بیشتر. این ماشین ها ستون فقرات هستند که کارایی و ثبات را در خط تولید دارو ایجاد می کنند.
عمل تولید خوب (GMP) با حصول اطمینان از اینکه داروها به طور مداوم مطابق با استانداردهای کیفیت دقیق تولید و کنترل می شوند، نقشی اساسی در تولید دارو ایفا می کند., پوشش همه چیز از مواد اولیه و تجهیزات گرفته تا پرسنل, رویه ها, و مستندات. با توجه به سازمان بهداشت جهانی, GMP برای به حداقل رساندن خطراتی مانند آلودگی طراحی شده است, برچسب گذاری نادرست, و خطاهای دوز مصرفی که تنها از طریق آزمایش محصول نهایی قابل حذف نیستند . به همین ترتیب, در ایالات متحده. سازمان غذا و داروی تاکید میکند که سیستمهای GMP تضمین میکنند که محصولات دارویی از استانداردهای لازم برای هویت برخوردارند, قدرت, کیفیت, و خلوص از طریق فرآیندهای کنترل شده و نظارت مستمر . با تعبیه کیفیت در هر مرحله از فرآیند تولید دارو, GMP نه تنها از ایمنی بیمار محافظت می کند، بلکه تولید کنندگان را قادر می سازد تا ثبات را حفظ کنند, رعایت, و دسترسی به بازار جهانی.
تولید دارو با چالش های پیچیده متعددی مواجه است, در درجه اول توسط الزامات نظارتی دقیق هدایت می شود, هزینه های بالای انطباق GMP, و نیاز به کیفیت محصول ثابت در سراسر بازارهای جهانی. تولیدکنندگان باید به طور مداوم خود را با مقررات در حال تحول سازمانهایی مانند FDA و WHO سازگار کنند و در عین حال از یکپارچگی دادهها اطمینان حاصل کنند., اعتبار سنجی فرآیند, و کنترل آلودگی, که پیچیدگی عملیاتی را به میزان قابل توجهی افزایش می دهد . علاوه بر این, بی ثباتی زنجیره تامین - مانند کمبود مواد خام, خطرات کیفیت API, و وابستگی به تامین کننده - می تواند مستقیماً تولید دارو را مختل کند و بر زمان بندی تحویل تأثیر بگذارد . بسیاری از شرکت ها نیز با تجهیزات قدیمی دست و پنجه نرم می کنند, اتوماسیون محدود, و نیاز به نیروی ماهر, همه اینها بر کارایی و انطباق تأثیر می گذارد . همانطور که صنعت تولید دارو به جهانی شدن ادامه می دهد, متعادل کردن کنترل هزینه, تضمین کیفیت, و رعایت مقررات یکی از بزرگترین چالش های جاری باقی مانده است.
صنعت داروسازی با ظهور داروسازی به سرعت در حال پیشرفت است 4.0, جایی که فناوری هایی مانند هوش مصنوعی, اتهام اتوماسیون, و اینترنت اشیا هوشمندتر را فعال می کنند, سیستم های تولید مبتنی بر داده که کارایی و کیفیت محصول را بهبود می بخشد . در همان زمان, تولیدکنندگان بیشتری برای دستیابی به تولید سریعتر، تولید مداوم را اتخاذ می کنند, کنترل کیفیت در زمان واقعی, و خروجی سازگارتر . این پیشرفت ها, همراه با افزایش تقاضا برای داروی شخصی و تولید پایدار, صنعت را به سمت انعطاف پذیری بیشتر سوق می دهند, خودکار, و مدل های تولید دارویی کارآمد.
تجهیزات پیچیده مورد استفاده در تولید دارو فقط برای نمایش نیست - مستقیماً کارایی و قابلیت اطمینان را افزایش می دهد.. در اینجا نحوه تفاوت ماشین آلات مدرن وجود دارد:

خلاصه, پیشرفته ماشین آلات دارویی به طور چشمگیری تولید را ساده می کند. تبدیل به چیزی می شود که قبلاً کار فشرده بود, فرآیندهای آهسته به سرعت بالا, گردش کار قابل اعتماد. همانطور که منابع ما نشان می دهد, استفاده از خطوط پیوسته و اتوماسیون منجر به خروجی و کیفیت بهتری می شود. نتیجه نهایی این است که تولیدکنندگان می توانند تقاضا را سریعتر و مداومتر برآورده کنند, با حفظ بالاترین استانداردهای کیفیت.
تولید دارو، پل حیاتی بین کشف دارو و مراقبت از بیمار است. این هنر و علم ساخت دارو است - تلاشی با فناوری بالا که نیاز به دقت دارد, پاکیزگی, و رعایت دقیق در هر مرحله. ما دیدیم که تولید دارو از مراحل کاملاً مشخصی پیروی می کند (از مواد اولیه گرفته تا بسته بندی) و از تجهیزات تخصصی برای ساخت مقادیر زیادی ایمن استفاده می کند, داروهای موثر. زیرا سلامت افراد به آن بستگی دارد, این صنعت به شدت تحت GMP تنظیم شده است تا کیفیت را حفظ کند. منتظر, پیشرفت هایی مانند تولید مداوم, اتهام اتوماسیون, و دیجیتالی شدن نوید این را می دهد که فرآیند را سریعتر و حتی قابل اطمینان تر کند.
با درک این فرآیندها و روندها, متخصصان صنعت می توانند از نحوه پرس کردن تجهیزات دارویی - قرص قدردانی کنند, دستگاه های تاول, مخلوط کن, و بیشتر - به کارایی و کیفیت کمک می کند. چه مهندس باشی, خریدار, یا تولید کننده در زمینه داروسازی, رعایت این اصول ضروری است.
اگر به دنبال ارتقا یا افزایش خط تولید داروی خود هستید, در نظر بگیرید که چگونه ماشین آلات و تخصص مناسب می تواند تفاوت ایجاد کند. برای قیمت با ما تماس بگیرید - تیم ما در Jinlupacking در ارائه راه حل های تجهیزات دارویی با کیفیت بالا و تجهیزات بسته بندی برای بهینه سازی فرآیندهای شما تخصص دارد..
تولید دارو فرآیند صنعتی تولید داروها از مواد خام به شکل های دوز نهایی مانند قرص است., کپسول ها, مایع, یا تزریقی. شامل فرمولاسیون است, پردازش, کنترل کیفیت, و بسته بندی تحت استانداردهای نظارتی دقیق برای اطمینان از ایمنی و اثربخشی.
تولید دارو ضروری است زیرا تضمین می کند که داروها به طور مداوم تولید می شوند, با خیال راحت, و در مقیاس. بدون آن, داروهای تولید شده در آزمایشگاه ها نمی توانند به طور قابل اعتماد به بیماران دسترسی پیدا کنند, فرم های قابل استفاده.
فرآیند تولید دارو معمولاً شامل:
• تهیه و آزمایش مواد خام
• توسعه فرمولاسیون
• ساخت و فرآوری
• کنترل و اعتبارسنجی کیفیت
• پر کردن و بسته بندی
• ذخیره سازی و توزیع
هر مرحله کیفیت محصول و مطابقت با استانداردهای نظارتی را تضمین می کند.
GMP (عمل تولید خوب) به مجموعه ای از مقررات اشاره دارد که تضمین می کند داروها به طور مداوم مطابق با استانداردهای کیفیت تولید و کنترل می شوند. به حداقل رساندن خطراتی مانند آلودگی کمک می کند, دوز نادرست, و خطاهای برچسب گذاری.
ماشین آلات دارویی رایج شامل:
• دستگاه های پرس تبلت
• دستگاه های پرکن کپسول
• میکسرها و گرانولاتورها
• ماشین آلات بسته بندی تاول
• ماشین های پرکن و لیبل زدن بطری
این ماشین ها کارایی را تضمین می کنند, دقت, و رعایت در تولید دارو.
• تولید دسته ای داروها را در مقادیر ثابت گام به گام تولید می کند.
• تولید مستمر بدون وقفه با جریان مواد در تمام مراحل اجرا می شود.
تولید مداوم کارایی و ثبات بالاتری را ارائه می دهد, در حالی که تولید دسته ای انعطاف پذیری را فراهم می کند.
API (ماده فعال دارویی) ماده اصلی در یک دارو است که اثر درمانی مورد نظر را ایجاد می کند. برای ایجاد فرم دوز نهایی با مواد کمکی ترکیب می شود.
برای اطمینان از ایمنی بیمار بسیار تنظیم شده است, کیفیت محصول, و قوام. سازمان های نظارتی برای جلوگیری از آلودگی به کنترل های دقیق نیاز دارند, اطمینان از دوز صحیح, و حفظ یکپارچگی محصول در طول تولید.
برای محافظت از داروها از تجهیزات بسته بندی دارویی استفاده می شود, اطمینان از دوز دقیق, و اطلاعات ضروری را ارائه دهید. ماشینهایی مانند بستهکننده تاولها و پرکنندههای بطری به حفظ ثبات محصول و بهبود انطباق بیمار کمک میکنند.
چالش های کلیدی عبارتند از:
• رعایت دقیق مقررات
• اختلالات زنجیره تامین
• هزینه های تولید بالا
• الزامات پیچیده کنترل کیفیت
• خطر آلودگی
این عوامل، تولید دارو را به یکی از پر تقاضاترین بخش های صنعتی تبدیل می کند.
مراجع:
1. تولید دارو - ویکی پدیا.
2.داروها: شیوه های تولید خوب - سازمان بهداشت جهانی.
3.روش تولید خوب فعلی (CGMP) مقررات - FDA.
4.تولید دارو & دستورالعمل های کیفیت - آژانس دارویی اروپا.

مد کوچک, بنیانگذار Jinlupacking, به ارمغان می آورد 30 سالها تخصص در بخش ماشین آلات دارویی. تحت رهبری او, جینلو تبدیل به یک تامین کننده قابل اعتماد با طراحی یکپارچه شده است, تولید, و فروش. پتی مشتاق به اشتراک گذاری دانش عمیق خود در صنعت است تا به مشتریان کمک کند تا پیچیدگی های بسته بندی دارو را طی کنند., اطمینان حاصل شود که آنها نه تنها تجهیزات را دریافت می کنند, اما یک مشارکت خدمات یک مرحله ای واقعی متناسب با اهداف تولید آنها.




حق چاپ © 2026 JinLuPacking.کلیه حقوق محفوظ است. عناصر & شرایط و سیاست حفظ حریم
پیوندهای دوستانه: بسته بندی غنی | تولید کنندگان دستگاه پرکن کپسول