
La fabrication pharmaceutique fait référence au processus à l’échelle industrielle consistant à transformer des ingrédients bruts en médicaments finis.. Autrement dit, c'est ainsi que les sociétés pharmaceutiques produisent des comprimés, gélules, injectables et autres formes galéniques dans des conditions strictement contrôlées. Ce processus implique une série d'étapes précises – du mélange des produits chimiques à la formation des pilules et à leur emballage – toutes conçues pour garantir la sécurité des médicaments finaux., efficace, et de haute qualité. Comme le note Petty Fu, la fabrication pharmaceutique « est le processus de synthèse à l’échelle industrielle, préparation, et le conditionnement de médicaments et de médicaments pharmaceutiques ». En pratique, c’est transformer les principes actifs pharmaceutiques (Apis) et excipients en formes posologiques (comme des tablettes, gélules, liquides, ou injectables) à travers diverses opérations unitaires (fraisage, granulation, compression, revêtement, remplissage aseptique, etc.) sous des réglementations strictes. L’objectif final est de produire à grande échelle des médicaments fiables tout en respectant toutes les normes d’hygiène et de sécurité..
La fabrication pharmaceutique n’est pas un simple mélange de produits chimiques : c’est un processus hautement technique.. À la base, cela implique: identifier ou synthétiser un ingrédient pharmaceutique actif (API), développer une formulation stable en mélangeant l'API avec d'autres matériaux (classeurs, charges, solvants, etc.), puis transformer ce mélange en une forme posologique finale. Chaque opération (mélange, granulation, séchage, compression, revêtement, remplissage, etc.) il faut le faire avec précision. La FDA et d’autres agences prennent ce processus très au sérieux : chaque lot doit répondre à des critères d’identité stricts., force, pureté, et qualité. En bref, la fabrication pharmaceutique est l’épine dorsale de l’industrie pharmaceutique, utiliser des machines spécialisées et des environnements contrôlés pour transformer de manière sûre et efficace des ingrédients chimiques en médicaments.

La fabrication pharmaceutique est l’une des industries les plus réglementées au monde. Pourquoi? Parce que nous fabriquons des produits que les gens vont injecter ou avaler, il est essentiel que chaque dose soit exactement correcte et exempte de contamination. Règlements (notamment GMP – Bonnes Pratiques de Fabrication) exister pour garantir la sécurité des patients et une qualité constante des produits. Par exemple, Les réglementations de la FDA exigent que les fabricants de médicaments suivent les bonnes pratiques de fabrication actuelles (cgMP), qui sont des lignes directrices pour garantir que les produits « sont systématiquement fabriqués et contrôlés selon les normes de qualité ». L'objectif est de garantir que chaque médicament:

En bref, parce que la vie des gens est en jeu, la fabrication de médicaments est régie par des règles rigoureuses émanant d'agences comme la FDA, Ema, et l'OMS. Ces règles couvrent tous les aspects – la conception des installations, équipement, formation du personnel, tests de matières premières, tenue de registres, nettoyage, validation, et plus. Par ici, les régulateurs contribuent à garantir que chaque pilule ou flacon qui parvient aux patients est fabriqué de manière à « garantir qu'un produit peut être utilisé sans danger ».
Le cheminement de la chimie brute à la médecine finale comporte plusieurs étapes clés. Bien que les processus spécifiques varient selon le produit, un flux de travail typique de fabrication pharmaceutique comprend ces étapes principales:
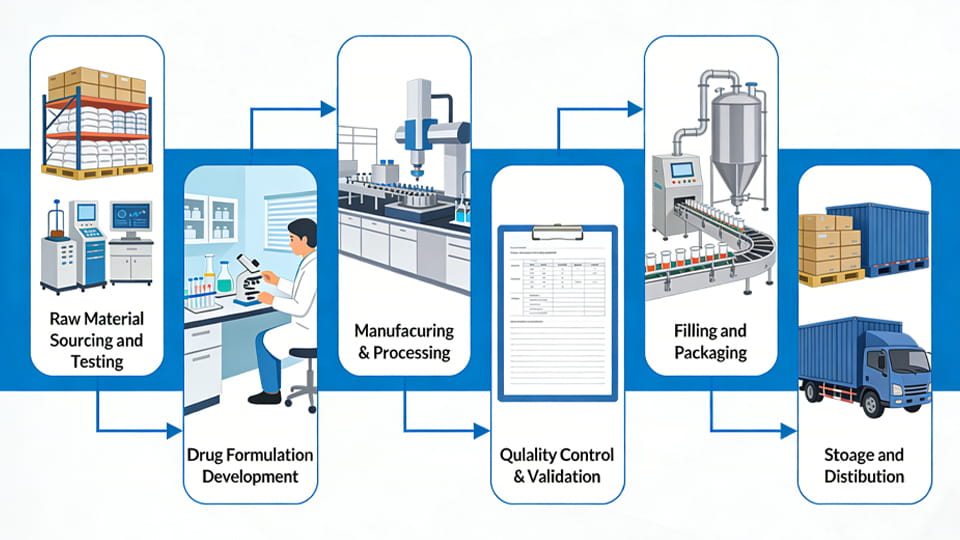
À travers toutes ces étapes, le strict respect des BPF est appliqué. Des audits fournisseurs en étape 1 aux contrôles de stérilité en étape 6, la qualité est intégrée à chaque étape. Ce processus en plusieurs étapes – des matières premières à la livraison finale – définit la fabrication pharmaceutique moderne.
Les usines pharmaceutiques peuvent être organisées de différentes manières en fonction du produit et de l'échelle.. Les principaux types d’approches de fabrication sont:
Traditionnellement, la plupart des produits médicamenteux ont été fabriqués par lots. Dans un processus par lots, une quantité fixe (lot) du produit est fabriqué du début à la fin. Chaque étape est exécutée séparément sur un lot avant de passer à autre chose. Par exemple, une formule est mélangée dans un grand réservoir, granulé, séché, compressé en comprimés, puis ce lot de comprimés est emballé et testé. L’avantage de la fabrication par lots est la flexibilité: il est relativement facile de changer de formulation ou de modifier une étape pour un nouveau produit. Les premières usines pharmaceutiques préféraient cette solution car elle permettait des changements de processus simples et une documentation simple.. La production par lots implique chaque opération exécutée séparément en utilisant une quantité définie de matériaux, avec contrôles intermédiaires entre phases. En pratique, cela signifie qu'une fois qu'une phase est terminée, le matériau est échantillonné et testé avant de continuer.
Avantages de la production par lots: Modification facile des produits ou de la taille des lots, contrôle et traçabilité simples des processus, idéal pour les petites séries ou lorsque des changements fréquents sont nécessaires.
Inconvénients de la production par lots: Généralement plus lent et moins efficace pour les gros volumes – après chaque lot, l'équipement doit être nettoyé et préparé pour le prochain. Une manipulation plus manuelle augmente les risques d'erreur humaine. Il y a « de nombreuses opérations nécessaires pour gérer, magasin, et suivre les produits intermédiaires » en mode batch. Aussi, si une erreur est trouvée à la fin, le lot entier peut être mis au rebut (Par exemple, une erreur d'étiquette ou un échec de contrôle qualité sur les comprimés pourrait forcer l'élimination de tous les comprimés de ce lot).
Une approche émergente est fabrication continue. Au lieu de lots discrets, la fabrication continue permet aux matériaux de circuler sans arrêt à chaque étape. Les matières premières sont introduites à une extrémité de la chaîne de production et le produit fini sort constamment par l'autre.. Toutes les opérations de l'unité (mélange, granulation, compression, etc.) sont intégrés sur une seule ligne sous contrôle en temps réel. Les processus continus sont hautement automatisés, avec capteurs en ligne mesurant les paramètres (comme l'uniformité du mélange ou la dureté des comprimés) à la volée. Les avantages incluent un débit beaucoup plus élevé, des délais de production plus courts, et une qualité plus constante. La fabrication continue optimise la chaîne d’approvisionnement, améliore la robustesse du processus de fabrication et réduit ainsi les défaillances des produits. En fait, des recherches montrent que le traitement continu peut réduire de moitié de nombreux coûts, réduisant ainsi la variabilité des produits, temps de contrôle qualité, et consommation d'énergie par de larges marges (les estimations vont de 40% à 70% réductions). Par exemple, parce que les matériaux continuent de bouger, les problèmes n’affectent qu’une petite partie du produit: toute partie hors spécifications peut être détournée pendant que le reste continue. Agences de régulation (FDA, Ema, etc.) sont de plus en plus favorables à la fabrication continue – en 2022 l'ICH a même publié des lignes directrices (Q13) pour encourager son adoption.
Avantages de la fabrication continue: Plus d’efficacité et de débit, moins d'interventions manuelles, produit final plus uniforme, et une empreinte de production souvent plus petite. La surveillance de la qualité en temps réel signifie que les problèmes sont détectés immédiatement. Il permet également une mise à l'échelle rapide en allongeant simplement la ligne ou en ajoutant des lignes parallèles..
Inconvénients de la fabrication continue: Nécessite de lourds investissements en capital dans de nouveaux, équipements et systèmes de contrôle intégrés. Changer de produit ou de recette est plus difficile car la ligne est optimisée pour un processus spécifique. Une validation approfondie du processus et une approbation réglementaire sont nécessaires pour passer d'une configuration par lots éprouvée à une configuration continue. (les entreprises doivent prouver que le nouveau processus donne le même résultat). Comme indiqué, l’adoption a été lente en partie à cause de ces défis.
| Aspect | Fabrication par lots | Fabrication continue |
|---|---|---|
| Style de production | Exécutions discrètes lot par lot | En cours, flux continu |
| Flexibilité | Élevé – facile à modifier les produits ou la taille des lots | Inférieur – optimisé pour un produit, moins de changements |
| Débit | Inférieur – temps d’arrêt nécessaire entre les lots | Plus élevé – rendement stable, des délais de livraison plus courts |
| Contrôle de qualité | Échantillonnage et tests étape par étape | Surveillance en ligne et contrôle de rétroaction |
| Risque de variabilité | Plus élevé – chaque lot peut différer du précédent | Inférieur – cohérence intégrée (seulement une petite partie mise au rebut en cas de problème) |
| Exemples de produits | De nombreux médicaments plus anciens, lots de petits volumes, fournitures cliniques | Formes posologiques solides à grand volume (comprimés, gélules), API par chimie de flux |
Une autre distinction clé est de savoir si le produit doit être stérile. La fabrication stérile s’applique aux injectables (vaccins, Médicaments IV, gouttes pour les yeux) and implantables. Ces produits ne tolèrent aucune contamination microbienne. Par conséquent, les lignes pharmaceutiques stériles fonctionnent dans des conditions extrêmement strictes (salles blanches de haute qualité, filtration de l'air, matériel stérilisé). Par exemple, les produits injectables nécessitent souvent des environnements de salle blanche ISO-5 (classe A/B en termes de BPF de l'UE) et processus de remplissage aseptique. Chaque flacon ou seringue est rempli sous des hottes à flux laminaire stériles ou dans des récipients pré-stérilisés, et composants (aiguilles, filtres) sont désinfectés. Par contre, la fabrication non stérile comprend des produits comme les comprimés, gélules, ondage, et liquides oraux qui ont des limites acceptables pour le contenu microbien (régi par les normes de la pharmacopée). Les lignes non stériles sont toujours très propres, mais ils ne nécessitent pas de conditions aseptiques totales. Les contrôles de qualité se concentrent davantage sur l'uniformité et la stabilité plutôt que sur la stérilité absolue.. En résumé, les processus stériles sont plus complexes et plus coûteux (en raison des besoins supplémentaires en matière de stérilisation et de salle blanche), alors que les processus non stériles, tout en restant réglementé, sont un peu plus simples.
La fabrication de produits pharmaceutiques peut également être classée par forme posologique:
Chaque type (solide, liquide, injectable) a ses propres nuances de processus, mais tous doivent être conformes aux BPF. Le choix du type de fabrication dépend de la forme et de l’utilisation du médicament.. Par exemple, vaccins (injectable) passer par des processus stériles plus élaborés qu'un comprimé à usage oral.
La fabrication pharmaceutique moderne repose sur un large éventail de machines spécialisées. L'équipement entre largement dans ces catégories:
Chaque équipement est conçu pour répondre aux normes pharmaceutiques (pièces de contact en acier inoxydable, possibilité de nettoyer facilement, et ainsi de suite). Principaux fabricants d'équipements pharmaceutiques (comme Jinlupacking) produire des machines telles que des presses à comprimés, charges de capsule, emballeurs de blisters, machines à compter, encartonneuses, et plus. Ces machines constituent l'épine dorsale de l'efficacité et de la cohérence de la chaîne de production pharmaceutique..
Bonne pratique de fabrication (GMP) joue un rôle central dans la fabrication pharmaceutique en garantissant que les médicaments sont systématiquement produits et contrôlés selon des normes de qualité strictes, couvrant tout, des matières premières et équipements au personnel, procédures, et documentation. Selon le Organisation Mondiale de la Santé, GMP est conçu pour minimiser les risques tels que la contamination, étiquetage incorrect, et erreurs de dosage qui ne peuvent être éliminées par les seuls tests du produit final . De la même manière, le NOUS. Administration des aliments et des médicaments souligne que les systèmes BPF garantissent que les produits pharmaceutiques répondent aux normes d'identité requises, force, qualité, et pureté grâce à des processus contrôlés et une surveillance continue . En intégrant la qualité à chaque étape du processus de fabrication pharmaceutique, Les BPF garantissent non seulement la sécurité des patients, mais permettent également aux fabricants de maintenir la cohérence, conformité, et accès au marché mondial.
La fabrication pharmaceutique est confrontée à de multiples défis complexes, principalement motivé par des exigences réglementaires strictes, coûts élevés de conformité aux BPF, et la nécessité d'une qualité de produit constante sur les marchés mondiaux. Les fabricants doivent continuellement s'adapter aux réglementations en évolution des agences comme la FDA et l'OMS tout en garantissant l'intégrité des données., validation du processus, et contrôle de la contamination, ce qui augmente considérablement la complexité opérationnelle . En outre, instabilité de la chaîne d'approvisionnement, comme les pénuries de matières premières, Risques liés à la qualité des API, et la dépendance aux fournisseurs – peuvent directement perturber la production pharmaceutique et avoir un impact sur les délais de livraison . De nombreuses entreprises sont également confrontées à des équipements obsolètes, automatisation limitée, et le besoin de personnel qualifié, qui affectent tous l’efficacité et la conformité . Alors que l’industrie pharmaceutique continue de se mondialiser, contrôle des coûts d’équilibrage, assurance qualité, et la conformité réglementaire reste l’un des plus grands défis permanents.
L'industrie pharmaceutique évolue rapidement avec la montée en puissance de l'industrie pharmaceutique. 4.0, où des technologies telles que l'IA, automation, et l'IoT permettent des solutions plus intelligentes, des systèmes de production basés sur les données qui améliorent l'efficacité et la qualité des produits . En même temps, de plus en plus de fabricants adoptent la fabrication continue pour accélérer la production, contrôle qualité en temps réel, et une sortie plus cohérente . Ces avancées, combiné à une demande croissante de médecine personnalisée et de production durable, poussent l’industrie vers plus de flexibilité, automatisé, et des modèles de production pharmaceutique efficaces.
Les équipements sophistiqués utilisés dans la production pharmaceutique ne sont pas seulement destinés au spectacle : ils améliorent directement l’efficacité et la fiabilité.. Voici comment les machines modernes font la différence:

En résumé, avancé machines pharmaceutiques rationalise considérablement la production. Cela transforme ce qui demandait autrefois beaucoup de travail, processus lents à grande vitesse, flux de travail fiables. Comme le montrent nos sources, tirer parti des lignes continues et de l’automatisation conduit à un rendement et une qualité nettement meilleurs. Le résultat final est que les fabricants peuvent répondre à la demande plus rapidement et de manière plus cohérente., tout en maintenant les plus hauts standards de qualité.
La fabrication pharmaceutique constitue le pont essentiel entre la découverte de médicaments et les soins aux patients. C’est l’art et la science de fabriquer des médicaments – un effort de haute technologie qui requiert de la précision., propreté, et une conformité stricte à chaque instant. Nous avons vu que la fabrication pharmaceutique suit des étapes bien définies (des matières premières à l'emballage) et utilise des équipements spécialisés pour fabriquer de grandes quantités de produits sûrs, médicaments efficaces. Parce que la santé des gens en dépend, l'industrie est étroitement réglementée par les BPF pour maintenir la qualité. Avoir hâte de, des avancées comme la fabrication continue, automation, et la numérisation promettent de rendre le processus plus rapide et encore plus fiable.
En comprenant ces processus et tendances, les professionnels de l'industrie peuvent apprécier la façon dont les équipements pharmaceutiques – presses à comprimés, machines à cloques, mélangeurs, et bien plus encore – contribue à l’efficacité et à la qualité. Que vous soyez ingénieur, acheteur, ou fabricant dans le domaine pharmaceutique, il est essentiel de respecter ces principes.
Si vous cherchez à mettre à niveau ou à faire évoluer votre ligne de production pharmaceutique, réfléchissez à la manière dont les bonnes machines et l’expertise peuvent faire la différence. Contactez-nous pour un devis – notre équipe chez Jinlupacking est spécialisée dans la fourniture de solutions d’équipements de fabrication et d’emballage pharmaceutiques de haute qualité pour optimiser vos processus.
La fabrication pharmaceutique est le processus industriel de production de médicaments à partir de matières premières sous des formes posologiques finies telles que des comprimés., gélules, liquides, ou injectables. Cela implique la formulation, traitement, contrôle de qualité, et emballage selon des normes réglementaires strictes pour garantir la sécurité et l'efficacité.
La fabrication pharmaceutique est essentielle car elle garantit la cohérence de la production des médicaments., sans risque, et à grande échelle. Sans ça, les médicaments développés en laboratoire ne pouvaient pas atteindre les patients de manière fiable, formulaires utilisables.
Le processus de fabrication pharmaceutique comprend généralement:
• Approvisionnement et tests de matières premières
• Développement de formulations
• Fabrication et transformation
• Contrôle qualité et validation
• Remplissage et emballage
• Stockage et distribution
Chaque étape garantit la qualité du produit et le respect des normes réglementaires.
GMP (Bonne pratique de fabrication) fait référence à un ensemble de réglementations qui garantissent que les médicaments sont systématiquement produits et contrôlés conformément aux normes de qualité. Il aide à minimiser les risques tels que la contamination, dosage incorrect, et erreurs d'étiquetage.
Les machines pharmaceutiques courantes comprennent:
• Presses à comprimés
• Machines de remplissage de gélules
• Mélangeurs et granulateurs
• Machines d'emballage sous blister
• Machines de remplissage et d'étiquetage de bouteilles
Ces machines assurent l'efficacité, précision, et conformité dans la production pharmaceutique.
• La fabrication par lots produit des médicaments en quantités fixes, étape par étape..
• La fabrication continue se déroule sans interruption avec des matériaux circulant à travers toutes les étapes.
La fabrication continue offre une efficacité et une cohérence supérieures, tandis que la fabrication par lots offre de la flexibilité.
API (Ingrédient pharmaceutique actif) est la substance principale d'un médicament qui produit l'effet thérapeutique souhaité. Il est combiné avec des excipients pour créer la forme posologique finale.
Il est hautement réglementé pour garantir la sécurité des patients, qualité du produit, et la cohérence. Les agences de réglementation exigent des contrôles stricts pour prévenir la contamination, assurer un dosage correct, et maintenir l'intégrité du produit tout au long de la production.
L'équipement d'emballage pharmaceutique est utilisé pour protéger les médicaments, assurer un dosage précis, et fournir des informations essentielles. Les machines telles que les emballeuses et les remplisseuses de bouteilles aident à maintenir la stabilité du produit et à améliorer l'observance des patients..
Les principaux défis comprennent:
• Conformité réglementaire stricte
• Perturbations de la chaîne d'approvisionnement
• Coûts de production élevés
• Exigences complexes en matière de contrôle de qualité
• Risque de contamination
Ces facteurs font de la fabrication pharmaceutique l’un des secteurs industriels les plus exigeants.
Références:
1. Fabrication pharmaceutique — Wikipédia.
2.Médicaments: Bonnes pratiques de fabrication - OMS.
3.Bonnes pratiques de fabrication actuelles (CGMP) Règlements — FDA.
4.Fabrication pharmaceutique & Directives de qualité — Agence européenne des médicaments.

Petit Fu, Fondateur de Jinlupacking, amène 30 années d'expertise dans le secteur des machines pharmaceutiques. Sous sa direction, Jinlu est devenu un fournisseur de confiance intégrant la conception, production, et ventes. Petty est passionné par le partage de ses connaissances approfondies de l'industrie pour aider ses clients à naviguer dans les complexités de l'emballage pharmaceutique., s'assurer qu'ils reçoivent non seulement du matériel, mais un véritable partenariat de services à guichet unique adapté à leurs objectifs de production.
Chaque produit et chaque usine ont leurs propres défis et situations en matière d'emballage.. Nous sommes là pour vous aider avec des machines de qualité garantie, solutions personnalisées, et les services les plus simples.
Inscrivez-vous pour recevoir le lancement de notre nouvelle machine et nos informations.
Droits d'auteur © 2026 JinLuPacking.Tous droits réservés. Termes & Conditions et politique de confidentialité
Liens amicaux: Emballage riche | Fabricants de machines de remplissage de capsules